พลังงานภายในร่างกายไม่สามารถเป็นค่าคงที่ได้ มันสามารถเปลี่ยนแปลงในร่างกายใดก็ได้ หากคุณเพิ่มอุณหภูมิร่างกายของคุณแล้วล่ะก็ พลังงานภายในจะเพิ่มขึ้นเพราะว่า ความเร็วเฉลี่ยของการเคลื่อนที่ของโมเลกุลจะเพิ่มขึ้น ดังนั้นพลังงานจลน์ของโมเลกุลของร่างกายจึงเพิ่มขึ้น และในทางกลับกัน เมื่ออุณหภูมิลดลง พลังงานภายในร่างกายก็จะลดลง
เราสามารถสรุปได้: พลังงานภายในของร่างกายเปลี่ยนแปลงหากความเร็วการเคลื่อนที่ของโมเลกุลเปลี่ยนไปลองพิจารณาว่าจะใช้วิธีใดเพื่อเพิ่มหรือลดความเร็วการเคลื่อนที่ของโมเลกุลได้ พิจารณาการทดลองต่อไปนี้ มาติดท่อทองเหลืองที่มีผนังบางเข้ากับขาตั้งกันดีกว่า เติมอีเทอร์ลงในหลอดแล้วปิดด้วยจุก จากนั้นเราก็ผูกมันด้วยเชือกและเริ่มขยับเชือกเข้าไปอย่างเข้มข้น ด้านที่แตกต่างกัน- หลังจากผ่านไประยะหนึ่ง อีเทอร์จะเดือด และพลังของไอน้ำจะดันปลั๊กออก ประสบการณ์แสดงให้เห็นว่าพลังงานภายในของสสาร (อีเทอร์) เพิ่มขึ้น หลังจากนั้นอุณหภูมิก็เปลี่ยนไปในขณะเดียวกันก็เดือด
พลังงานภายในที่เพิ่มขึ้นเกิดขึ้นเนื่องจากงานที่ทำเมื่อท่อถูกถูด้วยเชือก
ดังที่เราทราบ ความร้อนของร่างกายอาจเกิดขึ้นได้ในระหว่างการกระแทก การงอ หรือการยืดออก หรือพูดง่ายๆ ก็คือระหว่างการเปลี่ยนรูป จากตัวอย่างทั้งหมดที่ให้มา พลังงานภายในของร่างกายเพิ่มขึ้น
ดังนั้นพลังงานภายในร่างกายจึงสามารถเพิ่มขึ้นได้โดยการทำงานกับร่างกาย
หากร่างกายทำงานเอง พลังงานภายในจะลดลง
ลองพิจารณาการทดลองอื่น
เราสูบลมเข้าไปในภาชนะแก้วที่มีผนังหนาและปิดด้วยจุกปิดผ่านรูที่ทำขึ้นเป็นพิเศษ
หลังจากนั้นครู่หนึ่งจุกไม้ก๊อกก็จะลอยออกจากเรือ ทันทีที่จุกบินออกจากตัวเรือเราจะมองเห็นการก่อตัวของหมอก ผลที่ตามมาคือการก่อตัวของมันทำให้อากาศในถังเย็นลง อากาศอัดที่อยู่ในถังจะทำงานในระดับหนึ่งเมื่อดันปลั๊กออก งานนี้เขาแสดงเพราะพลังงานภายในของเขาซึ่งในเวลาเดียวกันก็ลดลง ข้อสรุปเกี่ยวกับการลดลงของพลังงานภายในสามารถสรุปได้จากการระบายความร้อนของอากาศในถัง ดังนั้น, พลังงานภายในร่างกายสามารถเปลี่ยนแปลงได้โดยการทำงานบางอย่าง
อย่างไรก็ตามพลังงานภายในสามารถเปลี่ยนแปลงไปได้อีกทางหนึ่งโดยไม่ต้องทำงาน ลองพิจารณาตัวอย่าง: น้ำในกาต้มน้ำที่วางอยู่บนเตากำลังเดือด อากาศตลอดจนวัตถุอื่นๆ ในห้องได้รับความร้อนจากหม้อน้ำส่วนกลาง ใน กรณีที่คล้ายกันพลังงานภายในเพิ่มขึ้นเพราะว่า อุณหภูมิร่างกายเพิ่มขึ้น แต่งานยังไม่เสร็จ ดังนั้นเราจึงสรุป การเปลี่ยนแปลงพลังงานภายในอาจไม่เกิดขึ้นเนื่องจากการปฏิบัติงานเฉพาะอย่าง
ลองดูอีกตัวอย่างหนึ่ง
วางเข็มถักโลหะลงในแก้วน้ำ พลังงานจลน์ของโมเลกุล น้ำร้อน, มากกว่า พลังงานจลน์อนุภาคโลหะเย็น โมเลกุลของน้ำร้อนจะถ่ายโอนพลังงานจลน์บางส่วนไปยังอนุภาคโลหะเย็น ดังนั้นพลังงานของโมเลกุลของน้ำจะลดลงในลักษณะใดลักษณะหนึ่ง ในขณะที่พลังงานของอนุภาคโลหะจะเพิ่มขึ้น อุณหภูมิของน้ำจะลดลง และอุณหภูมิของเข็มถักจะช้าลง  จะเพิ่มขึ้น ในอนาคตความแตกต่างระหว่างอุณหภูมิของเข็มถักกับน้ำจะหายไป จากประสบการณ์นี้ เราจึงเห็นการเปลี่ยนแปลงของพลังงานภายใน ร่างกายที่แตกต่างกัน- เราสรุป: พลังงานภายในของวัตถุต่างๆ เปลี่ยนแปลงเนื่องจากการถ่ายเทความร้อน
จะเพิ่มขึ้น ในอนาคตความแตกต่างระหว่างอุณหภูมิของเข็มถักกับน้ำจะหายไป จากประสบการณ์นี้ เราจึงเห็นการเปลี่ยนแปลงของพลังงานภายใน ร่างกายที่แตกต่างกัน- เราสรุป: พลังงานภายในของวัตถุต่างๆ เปลี่ยนแปลงเนื่องจากการถ่ายเทความร้อน
กระบวนการแปลงพลังงานภายในโดยไม่ต้องทำงานเฉพาะกับร่างกายหรือร่างกายเรียกว่า การถ่ายเทความร้อน
ยังมีคำถามอยู่ใช่ไหม? ไม่รู้จะทำการบ้านยังไง?
หากต้องการความช่วยเหลือจากครูสอนพิเศษ ให้ลงทะเบียน
บทเรียนแรกฟรี!
เว็บไซต์ เมื่อคัดลอกเนื้อหาทั้งหมดหรือบางส่วน จำเป็นต้องมีลิงก์ไปยังแหล่งที่มาดั้งเดิม
มีวิธีเปลี่ยนพลังงานภายในร่างกายได้หลายวิธี ได้แก่ งานและการถ่ายเทความร้อน
เมื่อทำงาน จะมีการเปลี่ยนแปลงในสองกรณี: ระหว่างการเสียดสีและระหว่างการเสียรูปที่ไม่ยืดหยุ่น เมื่องานเสร็จสิ้นด้วยแรงเสียดทาน พลังงานภายในจะเพิ่มขึ้นเนื่องจากการลดลง พลังงานกลร่างกายที่ถูก็ร้อนขึ้น ในกรณีของการบีบอัดร่างกายอย่างไม่ยืดหยุ่น พลังงานภายในของมันจะเพิ่มขึ้นเนื่องจากพลังงานกลลดลง
การถ่ายเทความร้อนเป็นกระบวนการของการเปลี่ยนแปลงพลังงานภายในโดยไม่ต้องทำงาน ในขณะที่พลังงานภายในของวัตถุหนึ่งเพิ่มขึ้นเนื่องจากพลังงานภายในของอีกวัตถุหนึ่งลดลง การเปลี่ยนแปลงพลังงานมาจากร่างกายมากขึ้น อุณหภูมิสูงไปยังร่างกายที่มีอุณหภูมิต่ำกว่า มีตัวเลือกต่างๆ: การนำความร้อน การพาความร้อน และการแผ่รังสี
~~~~~~~~~
พลังงานภายในไม่ใช่ค่าคงที่ มันอาจจะเปลี่ยนแปลง หากคุณเพิ่มอุณหภูมิของร่างกาย พลังงานภายในของมันจะเพิ่มขึ้น (ความเร็วเฉลี่ยของการเคลื่อนที่ของโมเลกุลจะเพิ่มขึ้น) เมื่ออุณหภูมิลดลง พลังงานภายในร่างกายจะลดลง
ลองพิจารณาประสบการณ์
มาติดท่อทองเหลืองที่มีผนังบางเข้ากับขาตั้งกันดีกว่า เติมอีเทอร์ลงในหลอดแล้วปิดด้วยจุก เรามัดมันด้วยเชือกและเริ่มขยับเชือกไปด้านข้างอย่างเข้มข้น หลังจากนั้นครู่หนึ่ง อีเธอร์จะเดือด และพลังของไอน้ำจะดันปลั๊กออกมา พลังงานภายในของสสาร (อีเทอร์) เพิ่มขึ้น: อุณหภูมิเปลี่ยนแปลง, เดือด พลังงานภายในที่เพิ่มขึ้นเกิดขึ้นเนื่องจากงานที่กำลังทำอยู่
ความร้อนของร่างกายอาจเกิดขึ้นได้ในระหว่างการกระแทก การงอ การยืดออก หรือการเสียรูป พลังงานภายในร่างกายเพิ่มขึ้น
พลังงานภายในร่างกายสามารถเพิ่มขึ้นได้โดยการทำงานกับร่างกาย หากร่างกายทำงานเอง พลังงานภายในจะลดลง
ลองพิจารณาประสบการณ์
เราสูบลมเข้าไปในภาชนะแก้วที่มีผนังหนาและปิดด้วยจุกปิดผ่านรูที่ทำขึ้นเป็นพิเศษ
หลังจากนั้นครู่หนึ่งจุกไม้ก๊อกก็จะลอยออกจากเรือ ในขณะที่จุกลอยออกจากตัวเรือ เราจะเห็นการก่อตัวของหมอก การก่อตัวของมันหมายความว่าอากาศในภาชนะเย็นลง อากาศอัดที่อยู่ในถังจะทำงานในระดับหนึ่งเมื่อดันปลั๊กออก เขาทำงานนี้เพราะพลังงานภายในของเขาลดลง ข้อสรุปเกี่ยวกับการลดลงของพลังงานภายในสามารถสรุปได้จากการระบายความร้อนของอากาศในถัง ดังนั้นพลังงานภายในร่างกายสามารถเปลี่ยนแปลงได้โดยการทำงานบางอย่าง
อย่างไรก็ตามพลังงานภายในสามารถเปลี่ยนแปลงไปได้อีกทางหนึ่งโดยไม่ต้องทำงาน
ลองดูตัวอย่าง
น้ำในกาต้มน้ำที่วางอยู่บนเตากำลังเดือด อากาศตลอดจนวัตถุอื่นๆ ในห้องได้รับความร้อนจากหม้อน้ำส่วนกลาง ในกรณีเช่นนี้พลังงานภายในจะเพิ่มขึ้นเพราะว่า อุณหภูมิร่างกายเพิ่มขึ้น แต่งานยังไม่เสร็จ ซึ่งหมายความว่าการเปลี่ยนแปลงพลังงานภายในอาจไม่เกิดขึ้นเนื่องจากการปฏิบัติงานบางอย่าง
ลองดูตัวอย่าง
วางเข็มถักโลหะลงในแก้วน้ำ พลังงานจลน์ของโมเลกุลน้ำร้อนมีค่ามากกว่าพลังงานจลน์ของอนุภาคโลหะเย็น โมเลกุลของน้ำร้อนจะถ่ายโอนพลังงานจลน์บางส่วนไปยังอนุภาคโลหะเย็น ดังนั้นพลังงานของโมเลกุลของน้ำจะลดลงในลักษณะใดลักษณะหนึ่ง ในขณะที่พลังงานของอนุภาคโลหะจะเพิ่มขึ้น อุณหภูมิของน้ำจะลดลง และอุณหภูมิของเข็มถักจะค่อยๆ เพิ่มขึ้น ในอนาคตความแตกต่างระหว่างอุณหภูมิของเข็มถักกับน้ำจะหายไป จากประสบการณ์นี้ เราจึงเห็นการเปลี่ยนแปลงของพลังงานภายในของร่างกายต่างๆ สรุปได้ว่า: พลังงานภายในของวัตถุต่างๆ เปลี่ยนแปลงเนื่องจากการถ่ายเทความร้อน
กระบวนการแปลงพลังงานภายในโดยไม่ต้องทำงานบางอย่างกับร่างกายหรือร่างกายเองเรียกว่าการถ่ายเทความร้อน
จากข้อมูลของ MKT สารทั้งหมดประกอบด้วยอนุภาคที่มีการเคลื่อนที่ด้วยความร้อนอย่างต่อเนื่องและมีปฏิกิริยาระหว่างกัน ดังนั้นแม้ว่าร่างกายจะไม่เคลื่อนไหวและมีพลังงานศักย์เป็นศูนย์ แต่ก็มีพลังงาน (พลังงานภายใน) ซึ่งเป็นพลังงานทั้งหมดของการเคลื่อนไหวและปฏิสัมพันธ์ของอนุภาคขนาดเล็กที่ประกอบกันเป็นร่างกาย พลังงานภายในประกอบด้วย:
- พลังงานจลน์ของการเคลื่อนที่แบบแปลน การหมุน และการสั่นของโมเลกุล
- พลังงานศักย์จากปฏิสัมพันธ์ของอะตอมและโมเลกุล
- พลังงานภายในอะตอมและพลังงานภายในนิวเคลียร์
ในอุณหพลศาสตร์ กระบวนการจะพิจารณาที่อุณหภูมิที่ การเคลื่อนไหวแบบสั่นอะตอมในโมเลกุลเช่น ที่อุณหภูมิไม่เกิน 1,000 เคลวิน ในกระบวนการเหล่านี้ พลังงานภายในเพียงสององค์ประกอบแรกเท่านั้นที่เปลี่ยนแปลง นั่นเป็นเหตุผล
ภายใต้ พลังงานภายในในอุณหพลศาสตร์เราเข้าใจผลรวมของพลังงานจลน์ของโมเลกุลและอะตอมทั้งหมดของร่างกายและพลังงานศักย์ของปฏิสัมพันธ์ของพวกมัน
พลังงานภายในของร่างกายจะกำหนดสถานะความร้อนและการเปลี่ยนแปลงระหว่างการเปลี่ยนจากสถานะหนึ่งไปอีกสถานะหนึ่ง ในสภาวะที่กำหนด ร่างกายจะมีพลังงานภายในที่แน่นอนอย่างสมบูรณ์ โดยไม่ขึ้นกับกระบวนการที่ร่างกายส่งผ่านเข้าสู่สภาวะนี้ ดังนั้นจึงมักเรียกว่าพลังงานภายใน การทำงานของสภาพร่างกาย.
\(~U = \dfrac (i)(2) \cdot \dfrac (m)(M) \cdot R \cdot T,\)
ที่ไหน ฉัน- ระดับความเป็นอิสระ สำหรับก๊าซเชิงเดี่ยว (เช่น ก๊าซมีตระกูล) ฉัน= 3 สำหรับไดอะตอมมิก - ฉัน = 5.
จากสูตรเหล่านี้จะเห็นได้ชัดเจนว่าพลังงานภายในของก๊าซในอุดมคติ ขึ้นอยู่กับอุณหภูมิและจำนวนโมเลกุลเท่านั้นและไม่ขึ้นอยู่กับปริมาตรหรือความดัน ดังนั้นการเปลี่ยนแปลงพลังงานภายในของก๊าซในอุดมคติจึงถูกกำหนดโดยการเปลี่ยนแปลงของอุณหภูมิเท่านั้นและไม่ขึ้นอยู่กับลักษณะของกระบวนการที่ก๊าซผ่านจากสถานะหนึ่งไปอีกสถานะหนึ่ง:
\(~\Delta U = U_2 - U_1 = \dfrac (i)(2) \cdot \dfrac(m)(M) \cdot R \cdot \Delta T ,\)
ที่ไหน Δ ต = ต 2 - ต 1 .
- โมเลกุลของก๊าซจริงมีปฏิกิริยาต่อกันจึงมีพลังงานศักย์ ว p ซึ่งขึ้นอยู่กับระยะห่างระหว่างโมเลกุลและปริมาตรที่ก๊าซครอบครอง ดังนั้นพลังงานภายในของก๊าซจริงจึงขึ้นอยู่กับอุณหภูมิ ปริมาตร และโครงสร้างโมเลกุล
*ที่มาของสูตร
พลังงานจลน์เฉลี่ยของโมเลกุล \(~\left\langle W_k \right\rangle = \dfrac (i)(2) \cdot k \cdot T\)
จำนวนโมเลกุลในแก๊สคือ \(~N = \dfrac (m)(M) \cdot N_A\)
ดังนั้นพลังงานภายในของก๊าซในอุดมคติคือ
\(~U = N \cdot \left\langle W_k \right\rangle = \dfrac (m)(M) \cdot N_A \cdot \dfrac (i)(2) \cdot k \cdot T .\)
เมื่อพิจารณาแล้วว่า k⋅Nก= รคือค่าคงที่ก๊าซสากลที่เรามี
\(~U = \dfrac (i)(2) \cdot \dfrac (m)(M) \cdot R \cdot T\) - พลังงานภายในของก๊าซในอุดมคติ
การเปลี่ยนแปลงพลังงานภายใน
เพื่อแก้ปัญหา ประเด็นการปฏิบัติไม่ใช่พลังงานภายในที่มีบทบาทสำคัญ แต่เป็นการเปลี่ยนแปลงΔ คุณ = คุณ 2 - คุณ 1. การเปลี่ยนแปลงพลังงานภายในคำนวณตามกฎการอนุรักษ์พลังงาน
พลังงานภายในร่างกายสามารถเปลี่ยนแปลงได้สองวิธี:
- เมื่อกระทำการ งานเครื่องกล- ก) หากแรงภายนอกทำให้เกิดการเสียรูปของร่างกาย ระยะห่างระหว่างอนุภาคที่วัตถุนั้นประกอบด้วยการเปลี่ยนแปลง และด้วยเหตุนี้พลังงานศักย์ของการโต้ตอบของอนุภาคจึงเปลี่ยนไป ในระหว่างการเสียรูปที่ไม่ยืดหยุ่นอุณหภูมิของร่างกายจะเปลี่ยนแปลงไปเช่น พลังงานจลน์ของการเคลื่อนที่ด้วยความร้อนของอนุภาคเปลี่ยนแปลงไป แต่เมื่อร่างกายผิดรูป งานก็เสร็จสิ้น ซึ่งเป็นการวัดการเปลี่ยนแปลงพลังงานภายในร่างกาย
- b) พลังงานภายในของร่างกายก็เปลี่ยนแปลงไปเช่นกันในระหว่างการชนที่ไม่ยืดหยุ่นกับวัตถุอื่น ดังที่เราเห็นก่อนหน้านี้ ในระหว่างการชนกันอย่างไม่ยืดหยุ่นของร่างกาย พลังงานจลน์ของพวกมันจะลดลง และกลายเป็นพลังงานภายใน (เช่น หากคุณตีลวดบนทั่งตีด้วยค้อนหลายครั้ง ลวดก็จะร้อนขึ้น) การวัดการเปลี่ยนแปลงในพลังงานจลน์ของร่างกายตามทฤษฎีบทพลังงานจลน์คือการทำงานของแรงกระทำ งานนี้ยังสามารถใช้เป็นการวัดการเปลี่ยนแปลงพลังงานภายในได้อีกด้วย c) การเปลี่ยนแปลงพลังงานภายในของร่างกายเกิดขึ้นภายใต้อิทธิพลของแรงเสียดทาน เนื่องจากดังที่ทราบจากประสบการณ์แล้ว แรงเสียดทานจะมาพร้อมกับการเปลี่ยนแปลงของอุณหภูมิของวัตถุที่ถูเสมอ งานที่ทำโดยแรงเสียดทานสามารถทำหน้าที่เป็นตัววัดการเปลี่ยนแปลงพลังงานภายในได้ด้วยความช่วยเหลือ
การแลกเปลี่ยนความร้อน - ตัวอย่างเช่น หากวางศพไว้ในเปลวไฟของเตา อุณหภูมิจะเปลี่ยน ดังนั้นพลังงานภายในก็จะเปลี่ยนไป อย่างไรก็ตาม ไม่มีงานทำที่นี่ เนื่องจากไม่มีการเคลื่อนไหวของร่างกายหรือส่วนต่างๆ ที่มองเห็นได้เรียกว่าการเปลี่ยนแปลงพลังงานภายในของระบบโดยไม่ต้องทำงาน
การแลกเปลี่ยนความร้อน
(การถ่ายเทความร้อน). การถ่ายเทความร้อนมีสามประเภท: การนำ การพาความร้อน และการแผ่รังสีก) การนำความร้อนคือกระบวนการแลกเปลี่ยนความร้อนระหว่างร่างกาย (หรือส่วนต่างๆ ของร่างกาย) ในระหว่างการสัมผัสโดยตรง ซึ่งเกิดจากการเคลื่อนตัวของอนุภาคในร่างกายอย่างวุ่นวายด้วยความร้อน แอมพลิจูดการสั่นสะเทือนระดับโมเลกุล
แข็ง ยิ่งอุณหภูมิยิ่งสูงขึ้น การนำความร้อนของก๊าซเกิดจากการแลกเปลี่ยนพลังงานระหว่างโมเลกุลของก๊าซในระหว่างการชนกัน ในกรณีของของเหลวกลไกทั้งสองทำงาน ค่าการนำความร้อนของสารมีค่าสูงสุดในสถานะของแข็งและค่าต่ำสุดในสถานะก๊าซข)
การพาความร้อน แสดงถึงการถ่ายเทความร้อนโดยการไหลของความร้อนของของเหลวหรือก๊าซจากบางพื้นที่ของปริมาตรที่พวกมันครอบครองไปยังพื้นที่อื่น c) การแลกเปลี่ยนความร้อนที่
รังสี
กระทำในระยะไกลด้วยคลื่นแม่เหล็กไฟฟ้า
เมื่อพิจารณาถึงกระบวนการทางอุณหพลศาสตร์ จะไม่พิจารณาการเคลื่อนที่ทางกลของมาโครบอดี้โดยรวม แนวคิดของการทำงานที่นี่เกี่ยวข้องกับการเปลี่ยนแปลงปริมาตรของร่างกายเช่น การเคลื่อนไหวของส่วนต่างๆ ของมาโครบอดี้ที่สัมพันธ์กัน กระบวนการนี้นำไปสู่การเปลี่ยนแปลงระยะห่างระหว่างอนุภาคและบ่อยครั้งยังทำให้เกิดการเปลี่ยนแปลงความเร็วของการเคลื่อนที่ด้วยเหตุนี้จึงเกิดการเปลี่ยนแปลงพลังงานภายในของร่างกาย
กระบวนการไอโซบาริก
ให้เราพิจารณากระบวนการไอโซบาริกก่อน ให้มีก๊าซอยู่ในกระบอกสูบโดยมีลูกสูบเคลื่อนที่ได้ที่อุณหภูมิ ต 1 (รูปที่ 1)
เราจะค่อยๆ ให้แก๊สร้อนจนถึงอุณหภูมิหนึ่ง ต 2. ก๊าซจะขยายตัวแบบไอโซแบริคัล และลูกสูบจะเคลื่อนที่จากตำแหน่ง 1 เพื่อวางตำแหน่ง 2 ไปเป็นระยะทาง Δ ล- แรงดันแก๊สจะทำงานต่อไป ร่างกายภายนอก- เพราะ พี= const แล้วตามด้วยแรงกด เอฟ = p⋅Sคงที่เช่นกัน ดังนั้นงานของแรงนี้สามารถคำนวณได้โดยใช้สูตร
\(~A = F \cdot \Delta l = p \cdot S \cdot \Delta l = p \cdot \Delta V,\)
ที่ไหน Δ วี- การเปลี่ยนแปลงปริมาณก๊าซ
- ถ้าปริมาตรของแก๊สไม่เปลี่ยนแปลง (กระบวนการไอโซคอริก) งานของแก๊สจะเป็นศูนย์
- แก๊สทำงานเฉพาะในกระบวนการเปลี่ยนปริมาตรเท่านั้น
เมื่อขยาย (Δ วี> 0) แก๊สเสร็จแล้ว การทำงานเชิงบวก (ก> 0); ระหว่างการบีบอัด (Δ วี < 0) газа совершается отрицательная работа (ก < 0).
- หากเราพิจารณาการทำงานของแรงภายนอก ก " (ก " = –ก) จากนั้นมีการขยายตัว (Δ วี> 0) แก๊ส ก " < 0); при сжатии (Δวี < 0) ก " > 0.
ให้เราเขียนสมการคลาเปรอง-เมนเดเลเยฟสำหรับสถานะก๊าซสองสถานะ:
\(~p \cdot V_1 = \nu \cdot R \cdot T_1, \; \; p \cdot V_2 = \nu \cdot R \cdot T_2,\)
\(~p \cdot (V_2 - V_1) = \nu \cdot R \cdot (T_2 - T_1) .\)
ดังนั้นเมื่อ กระบวนการไอโซบาริก
\(~A = \nu \cdot R \cdot \Delta T .\)
ถ้า ν = 1 โมล แล้วที่ Δ Τ = 1 K เราได้สิ่งนั้น รเท่ากับตัวเลข ก.
มันต่อจากนี้ ความหมายทางกายภาพค่าคงที่ก๊าซสากล: มีค่าเท่ากับงานที่ทำโดยก๊าซในอุดมคติ 1 โมล เมื่อได้รับความร้อนแบบไอโซบาริคัล 1 K
ไม่ใช่กระบวนการไอโซบาริก
บนแผนภูมิ พี (วี) ในกระบวนการไอโซบาริก งานจะเท่ากับพื้นที่ของสี่เหลี่ยมแรเงาในรูปที่ 2 ก
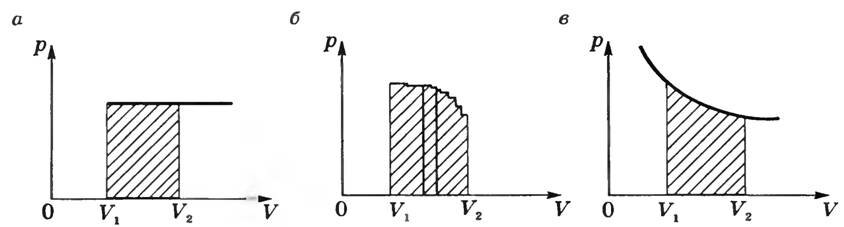
ถ้าเป็นกระบวนการ ไม่ใช่ไอโซบาริก(รูปที่ 2, b) จากนั้นกราฟฟังก์ชัน พี = ฉ(วี) สามารถแสดงเป็นเส้นประที่ประกอบด้วย ปริมาณมากไอโซชอร์และไอโซบาร์ งานในส่วนไอโซคอริกจะเป็นศูนย์ และงานรวมในส่วนไอโซบาริกทั้งหมดจะเท่ากับ
\(~A = \lim_(\Delta V \to 0) \sum^n_(i=1) p_i \cdot \Delta V_i\) หรือ \(~A = \int p(V) \cdot dV,\ )
เหล่านั้น. จะเท่ากัน พื้นที่ของร่างที่แรเงา.
ที่ กระบวนการไอโซเทอร์มอล (ต= const) งานจะเท่ากับพื้นที่ของรูปที่แรเงาแสดงในรูปที่ 2, c
เป็นไปได้ที่จะกำหนดงานโดยใช้สูตรสุดท้ายเฉพาะในกรณีที่ทราบว่าแรงดันแก๊สเปลี่ยนแปลงอย่างไรเมื่อปริมาตรเปลี่ยนแปลงเช่น ทราบรูปแบบของฟังก์ชันแล้ว พี = ฉ(วี).
ดังนั้น เป็นที่ชัดเจนว่าถึงแม้จะมีการเปลี่ยนแปลงปริมาตรของก๊าซเท่าๆ กัน งานจะขึ้นอยู่กับวิธีการเปลี่ยนผ่าน (เช่น ในกระบวนการ: อุณหภูมิคงที่ ไอโซบาริก...) จากสถานะเริ่มต้นของก๊าซไปยังขั้นตอนสุดท้าย สถานะ. ดังนั้นเราจึงสรุปได้ว่า
- งานในอุณหพลศาสตร์เป็นหน้าที่ของกระบวนการ ไม่ใช่หน้าที่ของสถานะ
ปริมาณความร้อน
ดังที่ทราบกันดีว่าในระหว่างกระบวนการทางกลต่างๆ การเปลี่ยนแปลงพลังงานกลจะเกิดขึ้น ว- การวัดการเปลี่ยนแปลงพลังงานกลคืองานของแรงที่ใช้กับระบบ:
\(~\เดลต้า W = A.\)
ในระหว่างการแลกเปลี่ยนความร้อน พลังงานภายในร่างกายจะเกิดการเปลี่ยนแปลง การวัดการเปลี่ยนแปลงพลังงานภายในระหว่างการถ่ายเทความร้อนคือปริมาณความร้อน
ปริมาณความร้อนคือการวัดการเปลี่ยนแปลงของพลังงานภายในระหว่างการถ่ายเทความร้อน
ดังนั้นทั้งงานและปริมาณความร้อนจึงเป็นลักษณะการเปลี่ยนแปลงของพลังงาน แต่ไม่เหมือนกับพลังงานภายใน พวกเขาไม่ได้ระบุลักษณะของระบบเอง (เช่นเดียวกับพลังงานภายใน) แต่กำหนดกระบวนการเปลี่ยนพลังงานจากประเภทหนึ่งไปอีกประเภทหนึ่ง (จากร่างกายหนึ่งไปยังอีกร่างกายหนึ่ง) เมื่อสถานะเปลี่ยนแปลงและขึ้นอยู่กับลักษณะของกระบวนการอย่างมีนัยสำคัญ
ความแตกต่างที่สำคัญระหว่างงานกับความร้อนก็คือ
- งานแสดงลักษณะของกระบวนการเปลี่ยนแปลงพลังงานภายในของระบบพร้อมกับการเปลี่ยนแปลงพลังงานจากประเภทหนึ่งไปเป็นอีกประเภทหนึ่ง (จากเครื่องกลไปเป็นภายใน)
- ปริมาณความร้อนเป็นลักษณะของกระบวนการถ่ายโอนพลังงานภายในจากร่างกายหนึ่งไปยังอีกร่างกายหนึ่ง (จากความร้อนมากขึ้นไปเป็นความร้อนน้อยลง) ซึ่งไม่ได้มาพร้อมกับการเปลี่ยนแปลงพลังงาน
เครื่องทำความร้อน (ความเย็น)
ประสบการณ์แสดงให้เห็นว่าปริมาณความร้อนที่ต้องใช้ในการทำความร้อนให้กับมวลกาย มเกี่ยวกับอุณหภูมิ ต 1 ถึงอุณหภูมิ ต 2 คำนวณโดยสูตร
\(~Q = c \cdot m \cdot (T_2 - T_1) = c \cdot m \cdot \Delta T,\)
ที่ไหน ค- ความจุความร้อนจำเพาะของสาร (ค่าตาราง)
\(~c = \dfrac(Q)(m \cdot \Delta T).\)
หน่วย SI ของความจุความร้อนจำเพาะคือจูลต่อกิโลกรัมเคลวิน (J/(kg K))
ความร้อนจำเพาะ คเป็นตัวเลขเท่ากับปริมาณความร้อนที่ต้องให้ร่างกายหนัก 1 กิโลกรัม เพื่อให้ความร้อน 1 เคลวิน
นอกจากความจุความร้อนจำเพาะแล้ว ยังพิจารณาปริมาณเช่นความจุความร้อนของร่างกายด้วย
ความจุความร้อนร่างกาย คตัวเลขเท่ากับปริมาณความร้อนที่ต้องใช้ในการเปลี่ยนอุณหภูมิของร่างกาย 1 K:
\(~C = \dfrac(Q)(\Delta T) = c \cdot m.\)
หน่วย SI ของความจุความร้อนของร่างกายคือ จูลต่อเคลวิน (J/K)
การกลายเป็นไอ (การควบแน่น)
ในการเปลี่ยนของเหลวให้เป็นไอที่อุณหภูมิคงที่ จำเป็นต้องใช้ความร้อนในปริมาณหนึ่ง
\(~Q = L \cdot ม.,\)
ที่ไหน ล- ความร้อนจำเพาะของการกลายเป็นไอ (ค่าตาราง) เมื่อไอน้ำควบแน่น ความร้อนจะถูกปล่อยออกมาในปริมาณเท่ากัน
หน่วย SI ของความร้อนจำเพาะของการกลายเป็นไอคือ จูลต่อกิโลกรัม (J/kg)
การหลอมละลาย (การตกผลึก)
เพื่อที่จะหลอมละลายร่างกายที่เป็นผลึกชั่งน้ำหนัก มเมื่อถึงจุดหลอมเหลว ร่างกายจำเป็นต้องสื่อสารปริมาณความร้อน
\(~Q = \แลมบ์ดา \cdot m,\)
ที่ไหน λ - ความร้อนจำเพาะของฟิวชัน (ค่าตาราง) เมื่อร่างกายตกผลึก ความร้อนจะถูกปล่อยออกมาในปริมาณเท่ากัน
หน่วย SI ของความร้อนจำเพาะของฟิวชันคือ จูลต่อกิโลกรัม (J/kg)
การเผาไหม้เชื้อเพลิง
ปริมาณความร้อนที่ปล่อยออกมาระหว่างการเผาไหม้เชื้อเพลิงโดยสมบูรณ์ ม,
\(~Q = q \cdot ม.,\)
ที่ไหน ถาม- ความร้อนจำเพาะของการเผาไหม้ (ค่าตาราง)
หน่วย SI ของความร้อนจำเพาะของการเผาไหม้คือ จูลต่อกิโลกรัม (J/kg)
วรรณกรรม
Aksenovich L. A. ฟิสิกส์ โรงเรียนมัธยมปลาย: ทฤษฎี. การมอบหมายงาน การทดสอบ: หนังสือเรียน เบี้ยเลี้ยงสำหรับสถาบันการศึกษาทั่วไป สิ่งแวดล้อม การศึกษา / L. A. Aksenovich, N. N. Rakina, K. S. Farino; เอ็ด เค.เอส. ฟาริโน. - Mn.: Adukatsiya i vyhavanne, 2004. - หน้า 129-133, 152-161.
เราพบว่าการระเหยของของเหลวเป็นไปได้ก็ต่อเมื่อมีความร้อนไหลไปยังของเหลวที่ระเหยเท่านั้น ทำไมจึงเป็นเช่นนี้?
ประการแรก ในระหว่างการระเหย พลังงานภายในของสารจะเพิ่มขึ้น พลังงานภายในของไออิ่มตัวจะมากกว่าพลังงานภายในของของเหลวซึ่งเป็นที่มาของไอนี้เสมอ การเพิ่มขึ้นของพลังงานภายในของสารในระหว่างการระเหยโดยไม่มีการเปลี่ยนแปลงอุณหภูมิเกิดขึ้นสาเหตุหลักมาจากการที่เมื่อมันผ่านเข้าไปในไอ ระยะห่างเฉลี่ยระหว่างโมเลกุลจะเพิ่มขึ้น ในเวลาเดียวกัน พลังงานศักย์ร่วมกันของพวกมันก็เพิ่มขึ้น เนื่องจากในการที่จะเคลื่อนโมเลกุลออกจากกันในระยะทางไกล จะต้องทุ่มเทงานเพื่อเอาชนะแรงดึงดูดของโมเลกุลซึ่งกันและกัน
นอกจากนี้ยังทำงานกับแรงกดดันภายนอกเนื่องจากไอน้ำมีปริมาตรมากกว่าของเหลวที่ก่อตัวขึ้น งานที่ทำในระหว่างการกลายเป็นไอจะชัดเจนเป็นพิเศษหากเราจินตนาการว่าของเหลวกำลังระเหยอยู่ในกระบอกสูบและไอน้ำที่เกิดขึ้นนั้นถูกยกขึ้นด้วยลูกสูบเบา (รูปที่ 492) ในขณะที่ทำงานต้านความดันบรรยากาศ งานนี้คำนวณง่าย มาคำนวณการต้มน้ำที่ความดันปกติและที่อุณหภูมิ ให้ลูกสูบมีพื้นที่ เพราะมันเป็นเรื่องปกติ ความดันบรรยากาศเท่ากันแล้วมีแรงกระทำต่อลูกสูบ ถ้าลูกสูบเพิ่มขึ้น งานก็จะเสร็จเรียบร้อย สิ่งนี้สร้าง ![]() คู่. ความหนาแน่นของไอที่ เท่ากับ ดังนั้น มวลไอจึงเท่ากับ ดังนั้นเมื่อไอน้ำเกิดขึ้น จะต้องทำงานกับแรงดันภายนอก
คู่. ความหนาแน่นของไอที่ เท่ากับ ดังนั้น มวลไอจึงเท่ากับ ดังนั้นเมื่อไอน้ำเกิดขึ้น จะต้องทำงานกับแรงดันภายนอก ![]() .
.
ข้าว. 492. ไอระเหยที่เกิดขึ้นจะยกลูกสูบ ในกรณีนี้ งานจะดำเนินการกับแรงกดดันภายนอก
เมื่อน้ำระเหย (ความร้อนจำเพาะของการระเหย) จะถูกใช้ไป ตามที่การคำนวณของเราแสดงให้เห็น สิ่งเหล่านี้ถูกใช้ไปกับการทำงานกับแรงกดดันจากภายนอก ดังนั้นส่วนที่เหลือเท่ากับแสดงถึงการเพิ่มขึ้นของพลังงานภายในของไอน้ำเมื่อเปรียบเทียบกับพลังงานของน้ำ อย่างที่คุณเห็นสำหรับน้ำ ความร้อนส่วนใหญ่ในระหว่างการระเหยไปเพื่อเพิ่มพลังงานภายในและมีเพียงส่วนเล็ก ๆ เท่านั้นที่ใช้ไปในการทำงานภายนอก
297.1. พิจารณาการเพิ่มขึ้นของพลังงานภายในระหว่างการระเหยของแอลกอฮอล์หากทราบว่าความหนาแน่นของไอของแอลกอฮอล์ที่จุดเดือดเท่ากับ .