Всем известны такие вещества, как графит и алмаз. Графит встречается повсюду. Например, из него делают стержни для простых карандашей. Графит - это вещество вполне доступное и дешевое. Но такое вещество, как алмаз, крайне отличается от графита. Алмаз - это самый дорогой камень, очень редкий и прозрачный, в отличие от графита. В это трудно поверить, но химическая формула графита совпадает с формулой алмаза. В данной статье мы разберем, как такое возможно.
Графит: история и свойства минерала
История графита насчитывает тысячи лет, поэтому точный год начала его применения установить крайне трудно. Графит знаменит тем, что хорошо проводит электрический ток. Кроме того, этот минерал является очень хрупким. Поэтому из него делают стержни для карандашей.
К химическим свойствам минерала можно отнести образование соединений включения со многими веществами, такими как соли и Минерал не растворяется в кислотах.
Формула графита - C, то есть он является одной из знаменитого шестого элемента таблицы Менделеева - углерода.

Алмаз: история и свойства минерала
История алмаза очень необычна. Считается, что первый алмаз был найден в Индии. В то время человечество так и не смогло понять всю силу этого камня. Геологам было лишь известно, что этот камень очень твердый и прочный. До 15 века алмазы стоили намного меньше, чем изумруды и рубины. И только потом неизвестный ювелир в процессе работы с камнем придал ему красивую огранку, которую позже стали называть бриллиантовой. Вот тогда-то камень и показал себя во всей своей красе.
Главным образом алмазы используют в промышленности. Этот минерал самый прочный на всем свете, именно поэтому из него делают абразивы, резцы для обработки прочных металлов и многое другое.
Как нам уже известно, формула графита в химии - C, такую же формулу имеет и алмаз.

Различия между алмазом и графитом
Несмотря на то что минералы имеют схожие химические формулы, они резко отличаются друг от друга как внешним видом, так и с химической точки зрения.
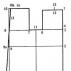
Прежде всего, алмаз и графит имеют совершенно различную друг от друга структуру. Ведь графит состоит из сетки шестиугольников, тогда как алмаз имеет кубическую кристаллическую структуру. Хрупкость графита обуславливается тем, что связь между его слоями нарушить очень легко, его атомы спокойно отделяются друг от друга. Из-за этого графит легко поглощает свет, сам он очень темный, в отличие от алмаза.
Отличается тем, что один атом углерода окружен еще четырьмя атомами в виде четырехгранного треугольника или пирамиды. Каждый атом находится на одинаковом расстоянии друг от друга. Связь у атомов очень крепкая, именно поэтому алмаз является таким твердым и прочным. Еще одно свойство алмаза - это то, что он может проводить свет, в отличие от графита.
Странно ли, что формула графита совпадает с формулой алмаза, но при этом минералы совершенно разные? Нет! Ведь алмаз создается природой при огромном давлении, а затем очень быстром охлаждении, тогда как графит возникает при низком давлении, но очень высокой температуре.

вещества?
Аллотропные вещества - это очень важное понятие в химии. Это основа основ, которая позволяет отличать вещества друг от друга.
В школе аллотропные вещества изучают на примере графита и алмаза, а также их различии. Итак, изучив различия алмаза и графита, можно сделать вывод, что аллотропия - это существование в природе двух и более веществ, которые различаются по своему строению и свойствам, но имеют схожую химическую формулу или относятся к одному химическому элементу.
Получение алмаза из графита
Формула графита - C - позволила ученым произвести множество опытов, вследствие чего были найдены аллотропные вещества графита.
Преподаватели рассказывают и школьникам, и студентам о том, как ученые пытались создать алмазы из графита. Эта история очень интересная и увлекательная, а еще она позволяет запомнить о существовании таких аллотропных веществ, как графит и алмаз, и об их различиях.
Некоторое время назад ученые пытались создать алмазы из графита. Они считали, что если формула алмаза и графита одинакова, то они смогут создать алмаз, ведь камень очень дорогой и редкий. Теперь мы знаем, что минерал алмаз появляется в природе при высоком давлении и мгновенном охлаждении. Поэтому ученые решили взорвать ѓрафит, тем самым создав нужные условия для образования алмаза. И на самом деле случилось чудо, после взрыва на графите образовались очень маленькие кристаллы алмаза.

Применение графита и алмаза
На сегодняшний день и графит, и алмаз используют главным образом в промышленности. Но примерно 10 % от всей добычи алмазов идет на ювелирное дело. Чаще всего из графита изготавливают карандаши, так как он очень хрупкий и ломкий, при этом оставляет следы.
Алмаз - самое твердое природное вещество. Кристаллы алмазов высоко ценятся и как технический материал, и как драгоценное украшение. Хорошо отшлифованный алмаз - бриллиант. Преломляя лучи света, он сверкает чистыми, яркими цветами радуги.
Размеры мировой добычи алмазов очень незначительны - гораздо меньше, чем благородных металлов - золота и платины. Из алмазов делают наконечники буров для сверления твердых горных пород. Также алмазы применяют для резки стекла и в виде “алмазного инструмента”(резцы, сверла, шлифовальные круги). Алмазным порошком шлифуют бриллианты и твердые сорта стали. Самый крупный из когда-либо найденных алмазов весит 602 г, имеет длину 11 см, ширину 5 см, высоту 6 см. Этот алмаз был найден в 1905 г и носит имя “Кэллиан”.
Один из самых крохотных в мире граненых алмазов, весом всего лишь 0,25 мг(в 4000 раз легче копеечной монетки), демонстрировался на всемирной выставке в Брюсселе. Несмотря на ничтожный вес и размер - зернышко объемом 0,07 мм3 ,- искусные руки гранильщика нанесли на нем на нем 57 граней, рассмотреть которые можно только под микроскопом.
В 1967 г. Б.В. Дерягин и Д.В. Федосеев вырастили на грани алмаза нитеобразный кристалл (“алмазные усы”). Рост происходил при высокой температуре, причем источником углерода служил метан; за четыре часа кристаллическая нить вырастала на 1 мм, что, вообще говоря, очень много для процессов такого рода.
Большая часть образцов аморфного угля состоит из искаженных кристаллов графита. Характерное расположение атомов углерода по углам шестиугольника при этом сохраняется.
В решетках графита часто встречаются разнообразные дефекты структуры, как структурные, так и химические, связанные с захватом ионов и атомов. В решетку графита могут внедряться (А. Убеллоде, Ф. Льюис) атомы бора, кислорода, серы и т. п., образующие связи между слоями и влияющие на проводимость графита. Графит образует своеобразные химические соединения, в которых присоединяющиеся частицы размещаются между плоскостями, занятыми атомами углерода.
При нагревании графита в парах щелочных металлов получаются легко окисляющиеся соединения. Так, при 400 °С калий образует соединение C8K. Состав соединений сильно зависит от температуры и изменяется в широких пределах. Известны соединения графита с рубидием, цезием; для натрия и лития четких результатов пока нет; натрий, по-видимому, дает соединение C64Na фиолетового цвета.
Графит дает также соединения с металлами, аммиаком и аминами типа MeC12(NH3)2. Решетка графита во всех случаях расширяется при образовании соединений, и межплоскостное расстояние достигает 0,66 нм, а для метиламинового комплекса лития даже до 0,69 нм. Получены соединения: C9Br, C5CI, C8CI, CF.
Тифлон (CF) серого цвета, изолятор, не похож на другие соединения типа соединений “внедрения”. Предполагается образование в нем ковалентных связей фтор - углерод.
Графит раньше применялся как пишущее средство. С XIX века и по сей день используют графитовые электроды в металлургии и химической промышленности, например в производстве алюминия: металл осаждается на графитовом катоде. Сейчас нашли применение графитизированные стали, то есть стали с добавлением монокристаллов графита. Эти стали используют при изготовлении коленчатых валов, поршней и других деталей, где особенно важна высокая прочность и твердость материала.
Графит играет важную роль в электротехнической промышленности и атомной энергетике, где его используют в качестве замедлителя нейтронов. С помощью графитовых стержней регулируют скорость реакции в атомных котлах.
Способность графита расщепляться на чешуйки позволяет делать на его основе смазочные вещества. Графит - прекрасный проводник теплоты, при этом он может выдержать значительные температуры до 3000 °С и выше. К тому же он химически довольно стоек. Эти свойства нашли применение в производстве графитовых теплообменников и в ракетной технике(для изготовления рулей и сопловых аппаратов.
Твердый, играющий на свету алмаз и непрозрачный, легко отслаивающийся графит образно можно назвать родными братьями. Ведь в химическом составе того и другого присутствует единственный элемент – углерод. Выясним, почему, имея общее происхождение, эти минералы настолько не похожи друг на друга и чем отличается алмаз от графита.
Определение
Алмаз – минерал, основой которого является углерод. Характеризуется метастабильностью, то есть способностью в обычных условиях неограниченно долго существовать в неизменном виде. Помещение алмаза в специфические условия, например в вакуум при повышенной температуре, приводит к его переходу в графит.
Алмаз
Графит – минерал, выступающий модификацией углерода. При трении от общей массы вещества отделяются чешуйки. Наиболее известное применение графита – изготовление из него карандашного грифеля.
 Графит
Графит Сравнение
Явление, при котором вещества имеют различные свойства, но образованы общим химическим элементом, называется аллотропией. Однако в природе, пожалуй, больше не найдется таких абсолютно разных аллотропных форм одного и того же элемента. Чем объясняется отличие алмаза от графита?
Решающую роль здесь играют особенности кристаллической структуры каждого из веществ. Скажем про алмаз. Связь между его атомами невероятно прочная. Это обусловлено способом их расположения относительно друг друга. Смежные атомные ячейки вещества имеют кубическую форму. Частицы расположены в углах ячеек, на их гранях и внутри них. Этот тип строения называется тетраэдрическим.
 Ячейка алмаза
Ячейка алмаза Такая геометрия атомов обеспечивает наиболее плотную их организацию, благодаря чему алмаз становится твердым, не поддающимся деформации. Вместе с тем это хрупкое вещество, способное раскалываться от удара. Строением также обуславливается высокая теплопроводность алмаза и свойство его кристаллов преломлять свет.
Графит обладает иной структурой. На атомном уровне он состоит из пластов, расположенных в разных плоскостях. Каждый пласт составляют примыкающие друг к другу шестиугольники, подобно сотам. Связь между атомами, которые являются вершинами шестиугольников, сильна только в пределах каждого слоя. А атомы, находящиеся в разных слоях, практически независимы друг от друга.
 Структура графита
Структура графита След от карандаша – это легко отделяемые слои графита. Вещество из-за особенностей строения поглощает свет, принимая достаточно невзрачный вид (но с металлическим блеском), и обладает электропроводностью.
Присущие минералам свойства определяют их пригодность в той или иной сфере. В чем разница между алмазом и графитом относительно их применения? Блистающий алмаз идеален для ювелирного производства. А твердость этого материала позволяет изготавливать из него качественные резцы по стеклу, суперпрочные сверла и другие востребованные изделия.
Графитовые стержни при протекании многих процессов играют роль электродов. Измельченный графит входит в состав минеральных красок и применяется как смазочный материал. А из смеси этого вещества и глины производят специальные емкости для плавки металлов.
Добыча алмазов, несомненно, достаточно прибыльный бизнес, который может поддержать экономику любой страны. Но тем не менее, наверняка многим предпринимателям хотелось бы снизить затраты на этих драгоценных камней и этим самым еще увеличить доход алмазодобывающей отрасли. А что, если возможно получать алмазы синтетическим способом из графита?
Чтобы ответить на этот вопрос, необходимо разобраться в природе двух материалов – и графита. Многие еще из уроков помнят, что эти два, казалось бы, таких разных материала целиком и полностью состоят .
Алмаз представляет собой обычно прозрачный кристалл, но может быть и синим, и голубым, и красным, и даже черным. Это самое твердое и прочное вещество на Земле. Такая твердость обусловлена особым строением кристаллической решетки. Она имеет форму тетраэдра, и все атомы углерода находятся на одном расстоянии друг от друга. Графит же темно-серый с металлическим отливом, мягкий и совершенно непрозрачный. Кристаллическая решетка графита расположена слоями, в каждом из которых молекулы собраны в прочные , однако между слоями связь молекул достаточно слабая. То есть, по сути, разница между алмазом и графитом заключается в различном строении кристаллической решетки.
Получение алмаза из графита
Как таковое превращение графита в алмаз возможно. Это доказали еще ученые ХХ века. В 1955 г. был представлен отчет компании General Electric и синтезированы первые алмазы, правда, очень мелкие. Первым осуществил синтез исследователь компании Т. Холл. Для достижения таких успехов было применено оборудование, позволяющее создавать давление в 120 тыс. атмосфер и температуру в 1800°С.
Группой ученых из Allied Chemical Corporation было осуществлено прямое превращение графита в алмаз. Для этого были использованы более экстремальные условия по сравнению с предыдущими методами. Для создания на 1 микросекунду предельного давления в 300 тыс. атмосфер и температуры в 1200°С применялось взрывчатое вещество огромной мощности. В результате в образце графита обнаруживалось несколько мелких частичек алмаза. Данные о результате эксперимента были опубликованы в 1961 г.
Однако это были не все способы получения алмазов из графита. В 1967 г. Р. Уэнторф вырастил первый алмаз на затравке. Скорость роста оказалась достаточно низкой. Самый крупный алмаз Р. Уэнторфа, изготовленный данным методом, достиг размера в 6 мм и веса в 1 карат (примерно 0,2 г).
Современные методы синтеза алмазов из графита
Современные технологии позволяют получать алмазы из графита несколькими методами. Алмазы синтезируются в условиях, максимально приближенных к природным, а также с использованием катализаторов. Производится наращивание кристаллов алмаза в метановой среде, а мелкую алмазную пыль для производства различных абразивов получают методом взрыва взрывчатых веществ или проволоки большим импульсом тока.
Источники:
- 1 Сравните строение алмаза и графита и их физические свойства: твердость, оптические свойства, электропроводность
- Народные изобретения, технологии - История и технология получения алмазов
Человек уже давно и близко знаком с таким веществом, как . Этот минерал обладает множеством полезных свойств, позволяющих применять его в самых разных областях, начиная с повседневной жизни и заканчивая сложными фабричными процессами.
Название «графит» произошло от , которое можно перевести с древнегреческого языка как «пишу», « ». Такое наименование обусловлено тем, что именно из графита изготавливаются стержни для карандашей, которые уже не одно помогают людям излагать свои мысли на бумаге, рисовать и делать наброски для живописных полотен. Цвет у графита темно-серый или серовато-черный, также это обладает характерным блеском, сродни металлическому.
Графит представляет собой одну из форм, которые может принимать углерод, в зависимости от того, каким способом связаны друг с другом атомы этого элемента. Графит очень хорошо проводит электричество и обладает высокой устойчивостью к тепловому воздействию, плавится он при температуре более 3500оС. Этот минерал слабо подвержен воздействию кислот, особенно при и средних температурах, а уровень его диамагнетизма существенно превосходит нормальные показатели.
Для прямого перехода графита в алмаз необходимы еще более экстремальные условия по сравнению с методикой, использующей металл-растворитель. Это связано с большой устойчивостью графита обусловленной очень прочными связями его атомов.
Результаты первых эскспериментов по прямому превращению графит—алмаз, выполненных П. Де-Карлн и Дж. Джеймисоном из «Аллайд кемикл Корпорэйпш», были опубликованы в 1961 г.
Для создания давления использовалось взрывчатое вещество большой мощности, с помощью которого в течение примерно миллионной доли секунды (одной -" микросекунды) поддерживалась температура около 1200° С и давление порядка 300000 атм. В этих условиях в образце графита после опыта обнаруживалось некоторое количество алмаза, правда в виде очень мелких частичек. Полученные кристаллиты по размерам (100 А=10 нм, или одна стотысячная доля миллиметра) сопоставимы с «карбонадо», встречающимся в метеоритах, образование которых объясняется воздействием мощной ударной волны, возникающей при ударе метеорита о земную поверхность.
В 1963 г. Фрэнсису Банди из «Дженерал электрик» удалось осуществить прямое превращение графита в алмаз при статическом Давлении, превышающем 130 000 атм . Такие давления были получены на модифицированной установке «белт» с большей внешней поверхностью поршней и меньшим рабочим объемом. Для создания таких давлений потребовалось увеличение прочности силовых деталей Установки.
Эксперименты включали искровой нагрев бруска графита до температур выше 2000° С. Нагревание осуществлялось импульсами электрического тока, а температура, необходимая для образования алмаза, сохранялась в течение нескольких миллисекунд (тысячных Долей секунды), т. е. существенно дольше, чем в экспериментах Де-Карли и Джеймисона.
Размеры новообразованных частиц были в 2—5 раз больше по сравнению с получающимися при ударном сжатии. Обе серии экспериментов дали необходимые параметры для построения фазовой диаграммы углерода, графически показывающей области температур и давлений, при которых стабильны алмаз, графит и расплав.I
Интересные эксперименты были проведены Банди и Дж. Каспером, которые использовали монокристаллы графита вместо ттоликрн-сталлического материала. Кристаллы алмаза в их первых опытах имели обычную кубическую кристаллическую структуру.
Еще Де-Карли и Джеймисон обратили внимание на то, что превращение в алмаз происходит легче, когда частички графита в образцах имеют удлинение вдоль так называемой оси с, т. е. перпендикулярно гексагональным слоям. Когда Банди и Каспер поместили монокристаллы таким образом, что давление прикладывалось вдоль оси с, и измерили электросопротивление кристаллов под давлением, то оказалось, что сопротивление увеличивается, когда достигается давление в 140 000 атм.
Это связывали с переходом графита в алмаз, хотя при снятии давления происходило обратное превращение в графит. Однако, когда эта процедура сопровождалась нагревом образца до 900 "С и выше, образовывались кристаллиты новой фазы высокого давления, имеющие гексагональную структуру, а не обычную — кубическую.
Гексагональный углерод также изредка находили в природных образцах, особенно в метеоритах. Он получил название лонсдеплит в честь Кэтлин Лонсдеил из Лондонского университета за ее большие заслуги в области кристаллографии, в частности в изучении алмаза.
В 1968 г. Г. Р. Коуэну. Б. В, Даннингтону и А. X. Хольцману нз компании «Дюпон де Немюр» был выдан патент на новый процесс, заключающийся в ударном сжатии металлических блоков, например железных отливок, содержащих небольшие включения графита (при давлениях, превышающих 1 млн. атм.)
Металл, у которого сжимаемость меньше, чем у графита, выполняет функции холодильника, очевь быстро охлаждающего включения.
Это предотвращает обратный переход алмаза, образовавшегося под действием ударной волны, в графит после прохождения этой волны—тенденции, характерной для экспериментов с монокристаллами при холодном сжатии. Конечный продукт, получаемый при использовании этой технологии, частично представлен гексагональным углеродом, что также подтверждает тенденцию к образованию лонсдейлита в условиях очень высоких давлений и относительно низких температур. Изготовленный таким способом материал используется в качестве шлифовального порошка.
Время от времени сообщается об исследованиях, направленных на модификацию того или иного из этих методов. Так, Л. Труеб применил принцип Де-Карли — Джеймисона для создания давления в 250 000—450 000 атм в течение 10—30 мкс, сопровождаемого разогревом после удара до 1100°С. Использовался графит в виде частичек диаметром 0,5—5 мкм, и получаемые алмазы имели те же размеры.
Однако установлено, что эти частички образованы очень мелкими (от Ю—40 до 100—1600 А) кубическими алмазами. В настоящее время нет сведений о том, что продукция «Аллайд кемикл корпорэйшн» поступает в коммерческую торговлю.
Способ, разработанный этой компанией, чтобы он мог успешно конкурировать с методом, использующим растноритель, и методом компании «Дюпон де Немюр», нуждается в дальнейшем совершенствовании. Потенциальное преимущество методов ударного сжатия в том, что взрыв—дешевый путь создания высоких давлений.
А чем графит отличается от алмаза?
И алмаз, и графит являются модификациями углерода.
Алмаз:
Графит:

Однако различий очень много:
1. Алмаз - самое твердое из известных веществ (10 по шкале Мооса), графит - одно из самых мягких (1-2).
2. Алмаз -
кристаллическая кубическая полиморфная модификация самородного углерода.
плотность около 3,5 г/куб.см, высокий показатель преломления среди драгоценных камней (2,417). полупроводник. крупные прозрачные кристаллы алмаза — драгоценные камни первого класса.
Графит - наиболее распространенная и устойчивая в земной коре полиморфная гексагональная модификация углерода. структура слоистая. плотность ок. 2,2 г/см3. огнеупорен, электропроводен, химически стоек.
3. Разница видна и при анализе создания искусственных алиазов: технология производства искусственных алмазов довольно сложна. синтезируют алмазы при температуре 1200-2000°С и давлении 1000-5000 МПа (50-60 тысяч атмосфер) из порошка графита, смешанного с порошкообразным железом, никелем, хромом. Кристаллизуются алмазы за счет того, что расплав при высоких давлениях не досыщен по отношению к графиту и пересыщен — по отношению к алмазам.
Кстати, графит тоже можно получить искусственным путем: нагревание антрацита без доступа воздуха.
4. Алмазы обычно люминесцируют в рентгеновских и ультрафиолетовых лучах. алмазы прозрачны для рентгеновских лучей. это облегчает идентификацию алмаза: некоторые стекла и бесцветные минералы, подчас внешне похожие на него, непрозрачны для рентгеновских лучей той же длины волны и интенсивности.
5. Насчет кристаллической решетки:

Разница видна невооруженным взглядом. Решетка алмаза очень прочная: атомы углерода находятся в ней по узлам двух кубических решеток с центрированными гранями, очень плотно вставленных одна в другую (а = 3,5595 А).
Насчет графита: связь между атомами прочная, ковалентного типа; между слоями - слабая, остаточно-металлического типа.